مقالات
فروزن سکشن
فروزن سکشن مغز
محققان علوم اعصاب معمولاً برای تعیین وضعیت جزئیات مغزی که زیر میکروسکوپ مشاهده می کنند، نیاز به دیدن برش هایی از کل مغز دارند. مغز باید سخت شود تا امکان گرفتن برش های نازک را به ما بدهد، مگر اینکه از میکروتوم تیغه ارتعاشی که بسیار کندتر است استفاده شود. قالبگیری در پارافین که معمولاً برای نمونه های پزشکی استفاده می شود فقط برای نمونه های کوچک یا نازک کار می کند،زیرا پارافین به مرکز کل مغز جوندگان نفوذ نمی کند بنابراین، محققان علوم اعصاب معمولا از انجماد برای سخت کردن بافت مغز برای برش استفاده می کنند.
از طرفی یخ زدگی به غشای سلولی آسیب می رساند و خوانایی بافتی نمونه های بیولوژیکی را کاهش می دهد. این بحث در مورد چرایی، عواقب، و چگونگی به حداقل رساندن یا جلوگیری از آسیب در هنگام استفاده از انجماد به عنوان وسیله ای برای سخت کردن بافت بیولوژیکی به منظور برش بخش های نازک برای بافت شناسی است.
اشکال مختلف آب در هنگام انجماد:
آب خالص می تواند در حالت جامد به سه شکل وجود داشته باشد. دو شکل کریستالی ، کریستال شش ضلعی و کریستال مکعبی و یا می تواند به سرعت منجمد شود که زمان تشکیل بلور را نداشته باشد و بی شکل می ماند (شکل زجاجیه). تشکیل کریستال دلیل انبساط آب در هنگام یخ زدن است (انبساط در انجماد ویژگی منحصر به فرد آب است)، بنابراین یخ زجاجیه پس از انجماد منبسط نمی شود. این باعث می شود که تنها شکل مطلوب انجماد برای نمونه های بیولوژیکی باشد.
نرخ انجماد بحرانی آب
گسترش محتوای آب و انبساط آن با انجماد، باعث کشیده شدن و نفوذ به غشای سلولی می شود. انجماد آهسته باعث تشکیل کریستال یخ میگردد. مواد بیولوژیکی رسانای حرارتی ضعیفی هستند برخی از کریستال های یخ در داخل هر قطعه بافت، بیش از 10 میلی متر از منبع سرد تشکیل شود. نمونهها روی سطح سرد قرار میگیرند تا منجمد شوند و این اتفاق به آرامی می افتد و بنابراین احتمالاً در قسمتهایی که دورتر از سطح انجماد هستند، کریستالهای یخ تشکیل میشوند. هنگامی که بلوک، برش داده می شود، تشکیل کریستال بزرگ، که به”پنیر سوئیسی”معروف اند سوراخ های متعدد و محتویات سلولی از دست رفته را به درجات مختلف، بسته به درجه و اندازه تشکیل کریستال، خواهد داشت.
توجه داشته باشید که میزان انجماد در ابتدای شروع فرایند اهمیت دارد نه دمای پایانی. انجماد سریع به درصد کل سطح در تماس با منبع سرد، حجم آب، دمای شروع آب (نمونه) و میزان سرد بودن منبع بستگی دارد. در حالت ایده آل، منبع سرما در دمای بسیار سرد قرار دارد و طوری تنظیم شده است که با تمام سطوح تماس داشته باشد.
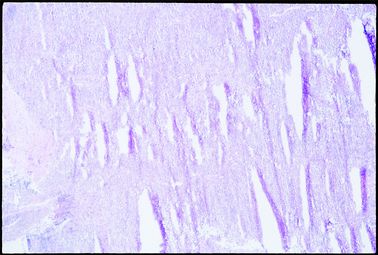
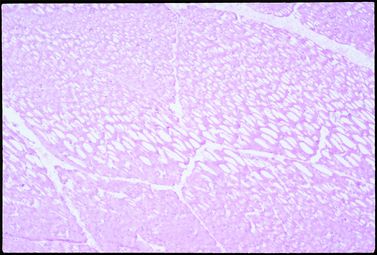
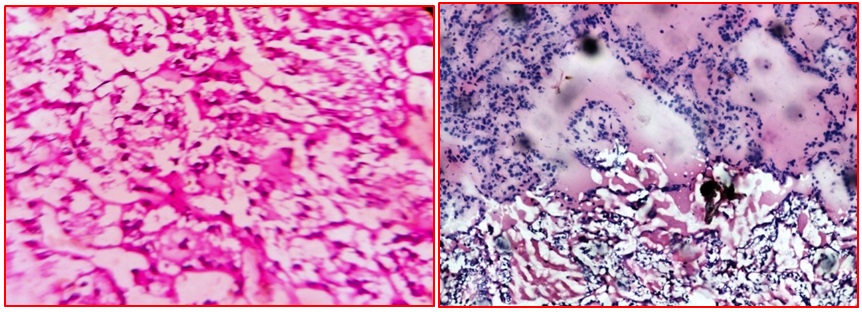
انجماد آهسته می تواند باعث تحریف و ایجاد تغییرات ناخواسته در بافت شود بطوریکه تاخیر در انجماد باعث تشکیل کریستال های یخ و جایگزینی آن مابین ساختار ذرات بافت شده و ظاهری شبیه به (Swiss Cheese) به آن میدهد.(مانند تصویر زیر )
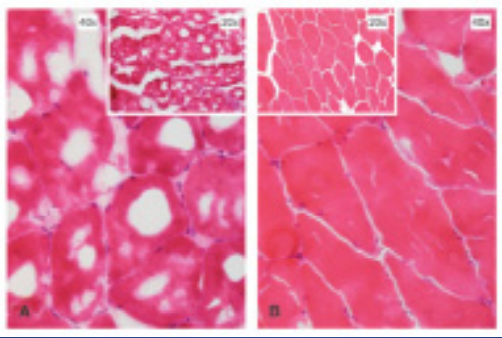
برش بافت در اسرع وقت
با این حال، حتی اگر یک نمونه با موفقیت به صورت شیشه ای منجمد شود، ممکن است در این حالت باقی نماند. یخ شیشه ای حالتی ناپایدار است. در دمای بالای 121- درجه سانتیگراد، یخ بی شکل به تدریج به شکل یخ مکعبی بازسازی می شود و منبسط می شود. در دمای بالای 80- درجه سانتیگراد، یخ مکعبی شروع به تغییر ساختار به صورت یخ شش ضلعی می کند و دوباره منبسط می شود. خوشبختانه، این یک فرآیند تبدیل آهسته است، بسته به گرادیان دما، و خلوص آب به ارامی صورت میگیرد.
در بیشتر کاربردهای معمول، بافت باید بالاتر از دمای انجماد فوری گرم شود تا برش داده شود (9- تا 19- درجه سانتی گراد برای مغز، اما بسته به نوع بافت متغییر است). در غیر این صورت برای بریدن بافت خیلی سرد است و با خم شدن و فشرده شدن توسط چاقو یا تیغ متلاشی می شود. علامت قابل مشاهده برش بیش از حد سرد، حالت کرکره ای” یا شکستگی های موازی با تیغه است. برش باید به محض گرم شدن بافت برای برش شروع شود. بافت هرگز نباید برای مدت طولانی در یک کرایواستات یا فریزر باقی بماند، حتی اگر چرخه یخ زدایی وجود نداشته باشد. تبدیل از یخ شیشه ای به کریستال های شش ضلعی بزرگ آغاز خواهد شد. سپس کریستال های یخ گسترش می یابند و به سلول ها آسیب می رسانند.
نیتروژن مایع
برای یخ زدن سریعتر، غوطه ور شدن در یک مایع بیشترین تماس سطحی را ایجاد می کند. دومین مورد قابل قبول این است که روی یک پایه فلزی از قبل سرد شده قرار دهید و به سرعت بافت را با یخ خشک که به صورت پودر درآورده شده تا تماس سطحی را به حداکثر برسانید، احاطه کنید.
نیتروژن مایع یکی از سردترین مایعاتی است که به طور معمول در دسترس است. با بافت مخلوط نمی شود. به نظر می رسد این ویژگی ها آن را به یک محیط انجماد ایده آل تبدیل می کند. با این حال، نیتروژن مایع، گرمای ویژه بسیار پایینی دارد. نتیجه این است که به صورت موضعی و فراوان در نقطه تماس حتی با یک تکه کوچک از بافت گرمتر می جوشد. پیامد این ویژگی این است که یک مانع بخار، یک لایه گاز نیتروژن، می تواند در کنار بافت ایجاد شود، و نفوذ سرما را به داخل بافت به شدت عایق کرده و در نتیجه سرعت انجماد را در یک الگوی غیرقابل پیش بینی کاهش می دهد. در نتیجه اغلب اتفاق می افتد که لایه بیرونی بافت سریع یخ زده و شیشه ای می شود، اما پس از آن سد بخار تشکیل می شود، سرما کندتر نفوذ می کند و قسمت داخلی کندتر یخ می زند.
تشکیل کریستال باعث انبساط بافت داخل پوسته یخ زده می شود و کل بلوک ترک می خورد. یک بلوک ترک خورده نشان می دهد که داخلی ترین قسمت بافت بصورت کریستالی منجمد شده است. توجه داشته باشید که این مشکل مربوط به بلوک های بزرگ بافت است (به عنوان مثال، مغز کامل رت یا حتی موش)، اما نیتروژن مایع برای انجماد بیوپسی یا نمونه های کوچکتر بسیار خوب عمل می کند و با موفقیت در آزمایشگاه های بافت شناسی بالینی استفاده می شود.
راه حل های دیگر
مایعات مختلف دیگر با اطمینان بیشتری برای بلوک های بزرگتر مورد استفاده قرار می گیرند، به ویژه ایزوپنتان که تا دمای 80- درجه سانتیگراد خنک شده است. سد بخار ایجاد نمیکند و اگر بافت کمی بیشتر از یک سانتی متر مکعب باشد،بصورت کاملا شیشه ای منجمد می شود. غوطه ور شدن کامل در مایع برای حداکثر تماس سطحی ضروری است و برای بافت بی ضرر است.
راه حل دیگر نفوذ یا پرفیوژن بافت با محلول های گلیسیرین، پلی اتیلن گلیکول (ضد یخ)، گلیسرول یا ساکارز است. اینها تشکیل کریستال را مختل می کنند و دمای انجماد را کاهش می دهند. ساکارز 30 درصد در بافر فسفات استفاده می شود، اما فقط با بافتی که بخوبی فیکس شده باشد، ، زیرا( اسمولاریته) ، باعث چروک شدن بافت میشود.
References
- Jongebloed, W.L., Stokroos, D., Kalicharan, D., and Van der Want, J.J.L. Is Cryopreservation Superior Over Tannic Acid/Arginine/Osmium Tetroxide non-Coating Preparation in Field Emission Scanning Electron Microscopy. Scanning Microscopy 13: 93-109, 1999.
- Reid N. and Beesley J. Sectioning and Cryosectioning for Electron Microscopy. Practical Methods in Electron Microscopy, Vol 13, Elsevier, Amsterdam